TAR: Cosa sono? Come si formano?
Scopriamo di più su queste specie condensabili prodotte nei processi di trattamento dei combustibili a base idrocarburica
L’obiettivo di questo articolo è fornirti informazioni sui TAR, ossia delle specie condensabili che si producono nei processi di trattamento (combustione, gassificazione, pirolisi) di combustibili a base idrocarburica. In particolar modo, l’articolo è strutturato in tre diverse aree:
- Introduzione alle reazioni di combustione. Quali sono i principali parametri che governano le reazioni di combustione? Perché possono formarsi delle specie inquinanti, quali i TAR? Cosa sono nello specifico i TAR?
- Fasi della combustione di una matrice solida. Quali sono i differenti fenomeni chimico-fisici che caratterizzano la combustione di una matrice solida? In quale fase si producono i TAR?
- Effetti dannosi dei TAR. Perché i TAR sono pericolosi? Che possibili conseguenze possono avere, se inalati?
Introduzione alle reazioni di combustione
Tra tutte le scoperte fatte dall’uomo, probabilmente una delle più significative è quella del fuoco. Il fuoco ha permesso ai nostri antenati di cuocere i cibi, di estendere le loro attività alle ore notturne, di proteggersi da animali predatori e di riscaldarsi nelle gelide notti invernali.
Oggi, come allora, i processi di combustione rivestono un’importanza fondamentale. È proprio grazie a questi processi che possiamo ammirare un allegro fuoco nel camino, che possiamo muoverci in macchina e che possiamo produrre energia elettrica nelle grandi centrali.
Nel ramo della produzione di energia elettrica, molto hanno fatto (e ancora oggi fanno) le fonti fossili. Accanto alle fonti fossili stanno sempre maggiormente prendendo piede le fonti rinnovabili, da sempre utilizzate e sempre più importanti per soddisfare il fabbisogno energetico globale.
In particolar modo, stanno emergendo delle tecnologie sempre più efficienti per il trattamento delle biomasse. Quando si parla di processi di combustione o gassificazione di biomasse (o di altri combustibili solidi), l’efficienza è di fondamentale importanza. Infatti le reazioni che avvengono sono estremamente complesse, e possono fornire come output una serie di specie chimiche che non rappresentano i tipici prodotti di combustione parziale o totale (CO, H2, CO2, H2O). Un attento controllo dei parametri di esercizio permette di incrementare notevolmente l’efficienza del sistema, in termini di performance energetiche e in termini di produzione di specie inquinanti.
In cosa consistono questi «parametri di esercizio»? Un parametro di fondamentale importanza, che ha importanti implicazioni nella formazione di inquinanti, è il rapporto combustibile/aria.
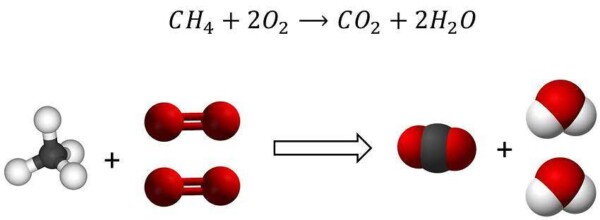
Per analizzare l’impatto di questo importante parametro, allontaniamoci momentaneamente dal mondo dei combustibili solidi e prendiamo in considerazione la specie idrocarburica più semplice: il metano. Il metano, per dare una reazione di combustione completa, ha bisogno di una ben definita quantità di ossigeno. In particolar modo, risulteranno necessarie due molecole di ossigeno per ciascuna molecola di metano.
Questa definita proporzione tra quantità di metano bruciato e ossigeno necessario viene definita rapporto stechiometrico della reazione di combustione completa. Le reazioni di combustione non sempre avvengono in condizioni stechiometriche: può esservi un eccesso o un difetto di aria.
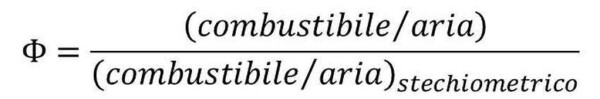
Per effettuare una stima quantitativa delle condizioni di combustione è stato introdotto un parametro, che viene denominato rapporto equivalente e che è definito a lato.
Sulla base delle condizioni operative possiamo distinguere tre diversi regimi:
- Se il rapporto equivalente è inferiore rispetto al valore unitario vuol dire che si è in condizioni di eccesso d’aria. Le condizioni di eccesso d’aria permettono di effettuare delle reazioni di combustione completa (in quanto l’ossigeno è sovra stechiometrico), ma possono comportare un abbassamento delle temperature di combustione. Infatti il comburente aggiuntivo, che non partecipa direttamente alla reazione di combustione, si comporta da volano termico ed assorbe parte del calore sprigionato dall’esotermicità del processo ossidativo.
- Se il rapporto equivalente ha valore unitario, il rapporto tra combustibile e aria rispetta la stechiometria, dunque la quantità di ossigeno presente è quella necessaria alla combustione totale dell’idrocarburo.
- Se il rapporto equivalente è superiore rispetto al valore unitario si ha un eccesso di combustibile. La quantità di aria presente non è sufficiente a permettere una combustione completa della matrice idrocarburica, e si avrà dunque una combustione parziale. Quando i valori del parametro sono significativamente maggiori rispetto al valore unitario, si ha una presenza predominante del combustibile, che in assenza di aria può decomporsi termicamente per effetto dei processi di pirolisi.
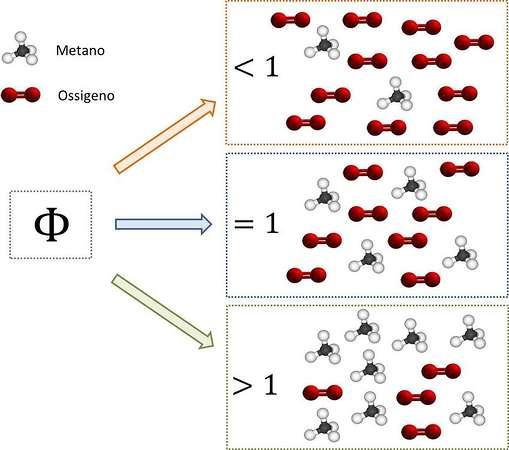
Ora che abbiamo definito le varie possibili condizioni operative, è di fondamentale importanza effettuare una precisazione. Se, ad esempio, alimentiamo una quantità di aria corrispondente a quella stechiometrica (Φ=1), non è detto che in tutto il volume in cui avviene la reazione di combustione il rapporto combustibile/aria sia pari a quello stechiometrico. Possono esservi infatti delle zone con eccesso di combustibile (Φ>1) e delle zone con carenza di combustibile (Φ<1), sulla base dei fenomeni di miscelazione. Ecco una condizione fondamentale: l’adeguata miscelazione tra combustibile e comburente. L’aspetto chimico delle reazioni di combustione è solo una faccia della medaglia: l’altra faccia corrisponde alle complicate fenomenologie di trasporto che avvengono.
Sulla base dei livelli di temperatura e di composizione locale, possono infatti formarsi specie inquinanti. Esaminiamo questo aspetto prendendo in considerazione la stessa molecola di prima (il metano), ed esaminando le complesse reazioni di natura radicalica che caratterizzano il suo processo di combustione .
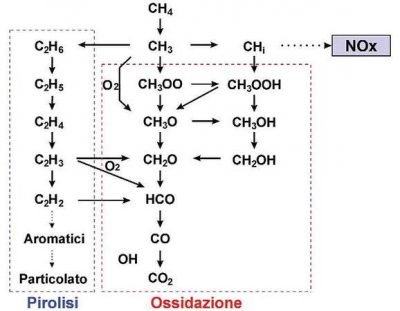
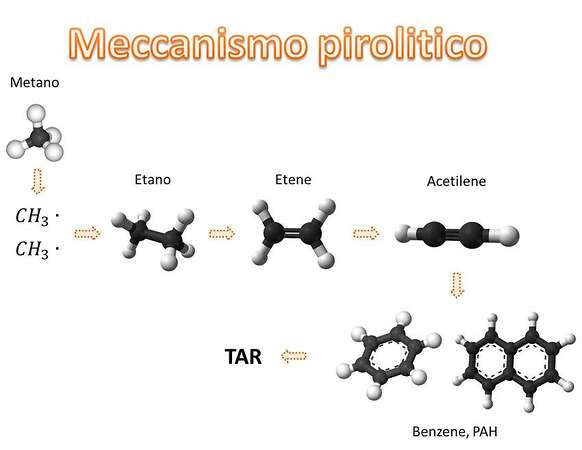
Come possiamo notare nell’immagine, il meccanismo di combustione del metano coinvolge una moltitudine di specie chimiche. In particolar modo, possiamo vedere come la presenza di ossigeno conduca all’ossidazione delle specie idrocarburiche, mentre la sua assenza conduca ad un meccanismo di natura pirolitica. Nel processo di natura pirolitica possiamo notare che la reazione di due radicali metilici (CH3) conduce alla formazione dell’etano (C2H6), il quale per successive reazioni di de-idrogenazione forma l’etene (C2H4) ed infine l’acetilene (C2H2). Quest’ultima specie contiene un triplo legame tra i due atomi di carbonio, e si comporta come precursore di specie aromatiche (benzene e PAH – Polyaromatic Hydrocarbons). È proprio in questo processo che avviene la potenziale formazione del TAR.
Questo termine sta ad indicare un’ampia classe di composti, liquefabili e prevalentemente idrocarburici, che si sviluppano in conseguenza a processi pirolitici ad elevata temperatura.
Abbiamo notato la complessità dei meccanismi cinetici della combustione/pirolisi del metano. Immagina come questa complessità incrementi ulteriormente, se consideriamo la combustione di specie idrocarburiche meno semplici! Se consideriamo la combustione di specie solide (quali le biomasse) o liquide, la descrizione del processo di combustione si rende ulteriormente più intricata a causa dei meccanismi di trasporto inter-fase. Infatti la mancata efficienza di questi processi può condurre alla genesi di zone pirolitiche, con conseguente formazione di TAR e soot (particolato).
Meccanismo di combustione di una biomassa solida legnosa
Una biomassa solida può essere descritta sulla base di tre componenti principali:
- Cellulosa: è una componente strutturale di fondamentale importanza nelle pareti cellulari delle piante. Risulta essere una catena polimerica che comprende fino a 10000 unità di molecole di D-glucosio.
- Emicellulosa: è una miscela complessa di diversi zuccheri (xilosio, mannosio, galattosio e arabinosio), dei quali tipicamente lo xilosio è il più abbondante.
- Lignina: è una macromolecola complessa, con massa molecolare molto elevata. Tende a conferire resistenza meccanica alla pianta.
Per capire come si comporta una biomassa in condizioni pirolitiche, si può analizzare come si comporta ciascuna delle sue componenti nelle medesime condizioni. Questa analisi può essere condotta sperimentalmente, e prende il nome di analisi termo-gravimetrica. Imponendo un certo tasso di riscaldamento del materiale, si registra come varia nel tempo la massa del materiale in questione. Man mano che aumenta la temperatura, si può notare come la massa della matrice solida diminuisca, e tendano invece a formarsi delle sostanze liquide e gassose. Questa è la conseguenza della depolimerizzazione delle catene che contraddistinguono le specie prima descritte. È proprio in questa fase che si ha la formazione del TAR, costituito da specie liquide o liquefabili provenienti dalla pirolisi della matrice solida.

Esaminando maggiormente nel dettaglio la combustione di una matrice solida, si possono riconoscere i seguenti passaggi:
- Disidratazione: quando il calore arriva alla particella, questa inizia ad incrementare la sua temperatura. In conseguenza all’incremento termico l’acqua presente nella matrice solida tende a transire in fase vapore, e si ha una conseguente diminuzione dell’umidità della particella stessa.
- Devolatilizzazione e processi pirolitici: come conseguenza del continuo aumento di temperatura, le molecole più volatili che caratterizzano la matrice solida tendono a passare in fase vapore. Si tratta sia di specie idrocarburiche semplici che di specie più complesse (PAH), alcune delle quali contraddistinguono proprio i TAR. In fase vapore avvengono dei fenomeni pirolitici secondari, che tendono a modificare ulteriormente la natura delle molecole descritte.
- Combustione in fase gassosa: se si ha un’adeguata miscelazione tra combustibile e comburente, le specie presenti in fase gassosa incontrano l’ossigeno e danno luogo a processi di ossidazione (che riscaldano le altre particelle presenti e fanno avvenire i fenomeni prima descritti). Senza un’adeguata miscelazione possono esservi delle zone a prevalenza idrocarburica, in cui non avvengono le reazioni di combustione. La mancata combustione può condurre alla permanenza delle specie idrocarburiche stesse. Queste possono dare luogo alla formazione di particolato.
- Combustione del char residuo: in conseguenza alla devolatilizzazione, la massa della matrice solida diminuisce e tende a rimanere un solido di natura carboniosa, denominato char. Un efficace contattatamento tra aria e char permette l’ulteriore ossidazione di quest’ultimo: alla fine di questo processo rimangono le ceneri, che non possono bruciare.
- Scarico delle ceneri: le ceneri rimaste vengono scaricate dalla caldaia o dal reattore, per consentire l’introduzione di nuovo materiale.Bene, abbiamo visto le fasi della combustione, comprendenti la formazione dei PAH e del TAR. La domanda che ora ci poniamo è: che effetti hanno questi composti sulla salute umana?
Effetti del TAR sulla salute umana
Quantificare gli effetti del TAR sulla salute umana risulta complesso. Un fattore che contribuisce alla complessità è sicuramente l’alto numero di specie che caratterizza il TAR: mentre alcune possono risultare innocue, altre possono essere potenzialmente pericolose.
Il benzene, ad esempio, è cancerogeno sia per gli uomini che per gli animali. Altri composti che caratterizzano il PAH, invece, hanno azione mutagena. Ad esempio il benzo(a)pirene, tramite azione del citocromo P-450, viene epossidato: tramite successive reazioni forma poi una specie che può reagire con il DNA, introducendo delle mutazioni.
La domanda sorge dunque spontanea: com’è possibile intervenire per rimuovere il TAR da correnti di processo?
Una risposta a questa domanda risiede sicuramente in un’azione preventiva, che consiste nell’effettuare una progettazione ottimale delle caldaie e dei reattori; questo permette di promuovere miscelazioni efficaci tra combustibili e comburenti.
Esistono anche dei metodi di post trattamento, che analizzeremo in un successivo articolo!
In attesa di nuove informazioni, guarda i nostri prodotti e le nostre Case History!
A presto!
Bibliografia
[1] A. D’Alessio, A. D’Anna, T. Faravelli e E. Ranzi, «Particolato fine e ultrafine,» Chimica & Ambiente, pp. 34-42, 2005.